医会在线
返回>清华大学祁海教授课题组发现虚拟记忆T细胞的活化新机制,为疫苗设计提供新思路
“同一个人不会遭受两次攻击",希腊历史学家修昔底德在描述雅典瘟疫时这样说道。
历史上,人类长期与细菌、病毒等有害微生物作斗争,仅天花这一种疾病所夺走的生命就远超两次世界大战的死亡人数总和。直到 18 世纪末,英国医生爱德华·詹纳偶然发现挤牛奶的女工不会感染天花,安全高效的天花预防方法由此出世。疫苗的出现**启人类医学新时代。
(来源:Pixabay)
千年后,人类已不再为天花这类传染病所困扰,但如今又遇到了新的敌人——新型冠状病毒。作为现阶段全球面临的最大难题之一,针对新型冠状病毒的疫苗研发已得到世界各地的响应,而对于疫苗研究来说,人体免疫系统的免疫记忆研究则是基础。
当病毒首次侵入人体时,免疫细胞会对病毒进行识别、活化、增殖、分化等一系列特异性反应,这些反应称为 “免疫应答”。当同一病毒再次入侵时,免疫系统便会根据 “记忆” 再次启动 “免疫应答” 杀死病毒,并且反应更为迅速、强烈和持久,这种现象称为 “免疫记忆”。免疫记忆是人体抵御病毒再次入侵的重要机制,能够有效防止同一疾病再次发生。
然而此前研究发现,有一类细胞即使没有经历过抗原特异的免疫反应,也会具有记忆细胞的特征,这类细胞被称为虚拟记忆 T 细胞(Virtual Memory T cells ,TVM)。研究者们发现虚拟记忆T细胞通过识别自身抗原产生。
在外来抗原刺激下,虚拟记忆T细胞具有与幼稚 T 细胞(TN)或真正记忆T细胞不同的功能特性,但其是否存在具有不同功能的亚群、多**状态的虚拟记忆T细胞如何参与组织区域免疫等问题,人们尚未找到答案。
近日,清华大学祁海教授课题组发现虚拟记忆T细胞的活化新机制,发现机体识别自身抗原产生的异质性虚拟记忆T细胞在区域组织免疫应答中介导先天性及获得性免疫反应新机制,为设计基于CD8+T细胞的对抗肺部感染的疫苗**新思路。
该项成果于近日以 Virtual memory T-cells orchestrate extra-lymphoid responsesconducive to resident memory 为题,发表在 Science Immunology 上。

(来源:ScienceImmunology)
祁海组研究者们使用流感病毒对无特殊病原体(SPF)的小鼠进行了肺部感染,研究者们发现,在感染后 18 小时之前小鼠体内便有大量的虚拟记忆T细胞入侵组织,这类细胞在早期入侵肺部的过程中具有显著优势。
由于细胞进行组织入侵依赖于趋化因子受体,研究者们通过体外筛选,还发现了虚拟记忆 T 细胞存在表达趋化因子受体 CCR2 的亚群。
为进一步探究这类虚拟记忆 T 细胞的功能,研究者们通过敲除小鼠**等方法,发现这些细胞在病毒感染早期具有非常重要的控制组织病毒载量的功能,这一功能主要是通过虚拟记忆T细胞抗原非特异的先天性免疫特征所实现。
传统上,T 细胞的活化需要经历一个相对漫长且复杂的过程:人体组织受到病原感染后,树突状细胞会捕捉到抗原,将其迁移并局部引流到淋巴结中,在淋巴结中活化幼稚 T 细胞,并进一步分化成为效应 T 细胞后,最终回到区域组织中,发挥免疫功能。
然而此次研究者们发现在小鼠感染早期,便有大量的虚拟记忆 T 细胞进入组织,因此他们猜测,这一多**的细胞群体很可能存在**型,由此可以直接并且快速地识别出组织中的抗原,并在组织中进行局部增殖,然后发育成为抗原特异的效应细胞。
他们最终通过抗体阻断并结合单细胞测序的方法证实了这一假说,发现早期入侵组织的多**虚拟记忆T细胞可以以次级淋巴器官非依赖的方式进行抗原特异增殖,揭示了一条T细胞活化的新途径。
紧接着,祁海组的研究者们通过多**及单**细胞过继转移实验,发现虚拟记忆 T 细胞具有可以产生组织驻留型记忆T细胞(tissue- resident memory T (TRM) )的能力,这种能力与传统幼稚细胞相比更强。
组织驻留性记忆 T 细胞是一个特殊的肿瘤浸润淋巴细胞(TIL)亚群,能够无限期地驻留在组织中,并迅速对同源抗原**出免疫反应。组织驻留性记忆 T 细胞最早在皮肤和肠道中被鉴定出来。
人体在初次免疫反应后会产生异质性的记忆 CD8+T 细胞,包括在血液组织间循环的效应记忆 T 细胞,在外周免疫器官中循环的中心记忆 T 细胞,和在组织中长期驻留的组织驻留性 T 细胞。
越来越多的证据表明组织驻留性T细胞在有效对抗组织区域感染过程中发挥至关重要的作用,但是该类细胞在初次免疫反应中的生成路径仍未为人所知。
祁海组的研究者们此次发现,早期进入组织中的 TVM 细胞在组织中局部增殖,并最终可以发育为组织驻留性记忆 T 细胞,由此揭示了组织驻留性记忆细胞生成的新路径。
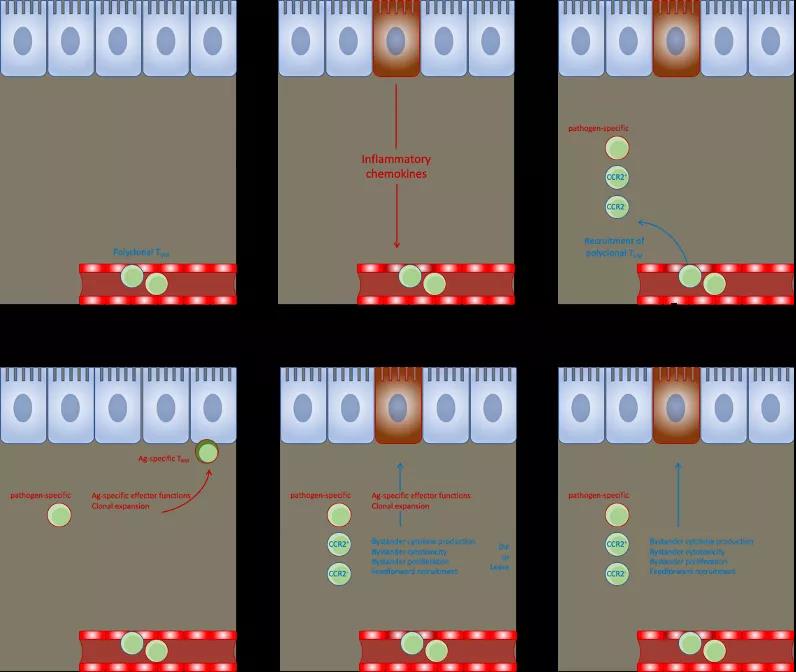
图 | TVM 细胞参与非淋巴组织内初次免疫应答并产生组织驻留型记忆细胞的模式图(来源:Science Immunology )
近期德尔塔病毒仍在全球范围内肆虐,全人类都面临着十分严峻的健康危机,祁海教授表示,团队所进行的基础研究可以为疫苗研发**另一种思路。
总结来说,此次祁海组研究者们发现了免疫记忆细胞新型异质性功能群体,揭示了机体利用自身免疫性产生的虚拟记忆 T 细胞对抗外来病原的新机制,虚拟记忆 T 细胞可以作为先天性与后天性免疫的桥梁,在免疫极早期进行巡逻监视,在效应期对病原体进行特异性**,此外还可以以强于幼稚细胞的优势发育为组织驻留性记忆细胞,由此对抗病毒的二次入侵,为设计细胞疫苗**新路径。
本次论文的通讯作者祁海教授于 2003 年毕业于德克萨斯州加尔维斯顿医学院,获病理学博士学位,主要从事免疫寄生虫学研究;2003 年 6 月至 2009 年 4 月在美国国立卫生研究院从事博士后研究,参与完善了基于双光子显微镜的在体免疫组织动态成像技术,主要关注体液免疫调节、多细胞在体交互作用机制、细胞与组织动态对免疫反应及记忆的影响。自 2009 年起,祁海教授任职于清华大学免疫研究所。
近年来,他在 Nature、Science 等顶级杂志上发表多项成果,在滤泡辅助 T 细胞和生发中心生物学方向获得突破性发现,为体液免疫调节研究领域**出了重要贡献。
对于中国目前的科研状况,祁海教授对 DeepTech 表示,虽然中国的科研传统较为薄弱,但这也意味着年轻的科学家们可以不用拘泥于太多框架,中国的研究者们更不会有太多包袱,西方国家长期积累的科研传统为他们的研究者带来诸多限制,而中国作为“后进生”往往可以跳脱出这些框架。
当前人才培养的平均水平在逐渐提高,祁海教授认为,在不断提升的过程中还需要创造高容忍度的创新环境以**人才个性化发展。
就免疫系统本身来说,其特点便是多样性,放大至整个科研领域来说,其未来发展同样是完全不可知的,这就需要人才培养既要能在某一领域上有所专攻,又要锻炼具有能应付多样性变化的基础能力。
祁海对 DeepTech 说道,就大环境来看,需要给科学家松绑,从社会组织角度来看,以组织为单位的科研是大头,社会需要更为完善的机制来为基础研究以及个人的研究发展**稳定、可靠的支持。