医会在线
返回>柳暗花明!Science:科学家解锁海量天然化合物宝库,已合成一种强大的抗生素

在浩瀚的历史长河中,细菌经历无数次“华山论剑”后使自己进化出能杀死“敌菌”的能力。上个世纪,细菌的这种独特能力被科学家利用并**发出曾经最强大的抗生素。
抗生素是微生物学史上最伟大的成就之一,它帮助人类治愈肺炎、葡萄球菌和肺结核等感染性疾病,使人类预期寿命从上个世纪**始延长了至少20年。然而,这个昔日的功臣已成为目前人类面临的十大公共卫生威胁之一。
数据显示,全世界每年有127万人死于耐药性细菌感染。如果不能**发出新的抗生素,因严重感染造成的发病率和死亡率还将进一步增加。预计到2050年,因无法治疗的感染造成的死亡人数将达到每年1000万人。
难道,我们就真的“山穷水尽”了吗?
显然不是。近日,发表在《Nature Biotechology》上的一项研究中,中国科学院微生物研究所王军研究员和陈义华研究员团队合作,利用机器学习方法,从一万多个肠道微生物中“海淘”出三个具有显著活性和安全性的抗菌肽“潜力股”。

2022年5月26日,发表在《Science》上的一项新研究又为解决全球抗生素耐药危机带来了曙光。来自洛克菲勒大学遗传编码小分子实验室负责人Sean Brady教授和中国药科大学王宗强教授等人使用生物信息学从海量细菌天然宝库中**了一种新的抗生素,它使用了全新的机制杀死了常见的耐药细菌。
Brady教授说:“这不仅仅是一个很酷的新分子,它是药物发现新方法的验证。这项研究是计算生物学、基因测序和**化学共同揭**细菌进化秘密的一个宝贵例子。”

微生物来源的活性天然产物是临床药物及其先导化合物的重要来源。依赖于实验室“分离、培养和发酵”的经典微生物药物研发模式,使研究人员可从可培养微生物(在实验室条件下可繁殖)中发现多种挽救人类生命和提高生活水平的治疗药物。
然而,传统的微生物药物研发模式导致了重复的化合物不断被发现,在浪费资源的同时,也面临着新骨架或新活性化合物来源枯竭的严重挑战。
随着基因测序技术的快速发展,科学家们发现自然界中超过99%的微生物为不可培养微生物,其基因组(宏基因组)编码的天然产物数量预计是可培养微生物的2至3个数量级,这是个浩大且极具吸引力的微生物药物天然宝库。
此前的细菌基因组测序工作发现了大量生物**基因簇(BGC),这些基因簇似乎不编码已知的天然产物,但可能包含抗生素生物**的遗传指令和具有不同的作用模式,从而有助于补充抗生素发现管道。不幸的是,大多数已测序的基因簇在实验室中保持沉默,它们编码的分子仍然是个谜。
在这项新研究中,研究人员**始在这个巨大的天然宝库中搜索那些从未被探索的细菌基因。“cil”基因簇因与其他参与**抗生素的基因接近,因此脱颖而出。他们使用“**生物信息学天然产物(synBNP)”的算法来预测潜在的化合物,并从中发现了一种天然脂肽类抗生素。研究人员将其命名为cilagicin。
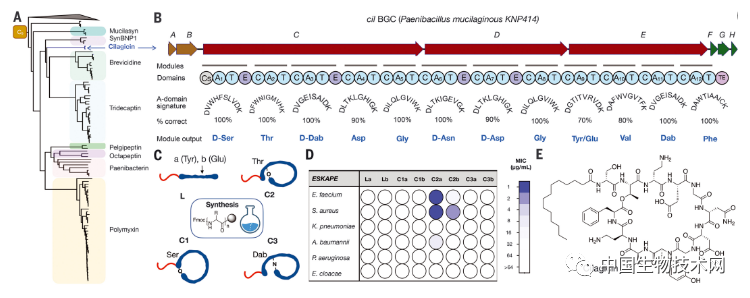
Cilagicin在实验室中可有效杀死了革兰氏阳性细菌,且不伤害人类细胞,并成功治愈了小鼠的细菌感染;cilagicin还能有效抑制耐甲氧西林金黄色葡萄球菌(MRSA)、艰难梭菌和其他几种致命的超级耐药细菌;而且,即使在对抗专门培养用于抗cilagicin的细菌面前,这种**化合物仍然占尽上风。
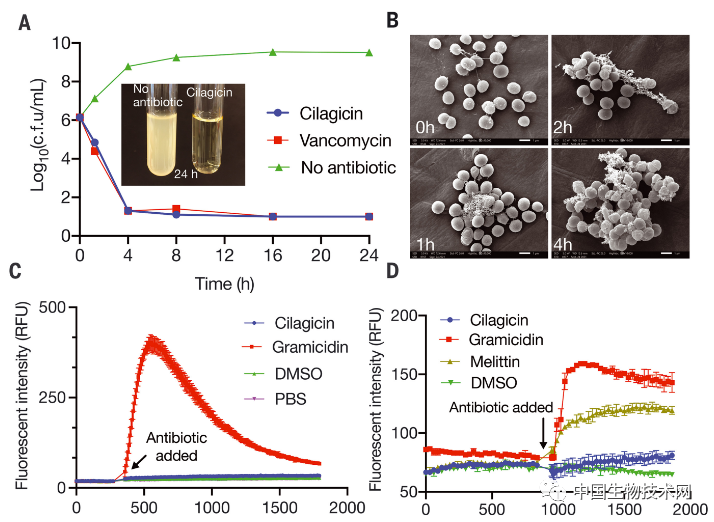
在实验中,研究人员发现在cilagicin**后的培养物中积累了细胞壁前体。这意味着,cilagicin可以抑制细胞壁的生物**。实验结果表明,cilagicin通过螯合脂质载体分子十一碳二烯磷酸(C55-P) 及其无活性形式的十一碳二烯焦磷酸(C55-PP)来抑制细胞壁的生物**。这两个分子都有助于维持细菌的细胞壁。现有抗生素(如杆菌肽)只能结合这两种分子中的一种,不能同时结合两种;而细菌通常可以通过利用剩余那个分子拼凑出一个细胞壁来抵抗这类药物。因此,cilagicin是具备了二合一的全新机成杀死了耐药菌。
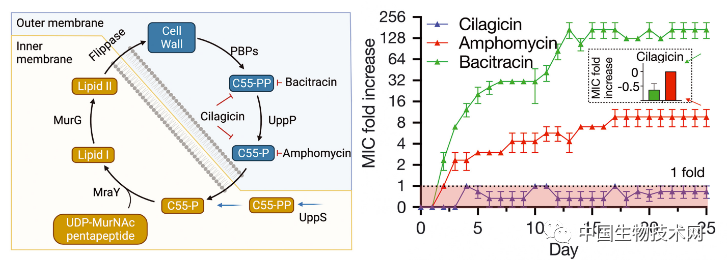
研究人员猜测,Cilagicin使这两种分子脱靶的能力可能会形成一个无法逾越的障碍,从而阻止耐药性的发生。
Brady表示,Cilagicin距离人体试验还有很长的路要走。在后续研究中,他们将进行进一步**以优化该化合物,并在动物模型中对更多的病原体进行测试,以确定Cilagicin在治疗哪些疾病方面可能最有效。
Brady说:“这项跨学科的研究工作是一个很好的例子,说明可以发现隐藏在基因簇中的东西。通过这种策略,我们现在可以解锁大量的新型天然化合物。希望这个令人兴奋的发现将**一个全新的候选药物库。”







